EXERCICE CORRIGE
L’analyse de l’eau d’un forage a donné le résultat suivant en mg/L, pH en unité pH et CE en µS/cm.
|
Ca2+ |
Mg2- |
Na+ |
K+ |
HCO-3 |
Cl- |
SO2-4 |
NO-3 |
PO3-4 |
CE |
pH |
pHs |
TDS |
|
106 |
35 |
44 |
0.82 |
312 |
42.60 |
97.80 |
17.60 |
0.15 |
864 |
7.40 |
7.65 |
864 |
A-) Déterminer le facies hydrochimique.
B-) Calculer Le TH à l’aide de la formule Sawyer McCarthy.
C-)
Comparer les Valeurs de l’analyse physico–chimique ave la norme de L’OMS.
Discuter le résultat.
D-) Calculer les paramètres suivants : SAR, %Na+, carbonate résiduel RSC et Mg ratio, PI. Quelles conclusions en tirez-vous ! Diagramme de richards et Wilcox
E- Cette eau est-elle utilisable industriellement.
Réponses
Avant de répondre à la question, il faut calculer la balance ionique. Elle permet de mettre en évidence la rentabilité de l’analyse et est donnée par la relation ci-dessous.
BI (%) = ∑r+ + ∑r- /∑r x100
La balance ionique calculée est de 8% inferieure a la valeur tolérée de 10 %. Donc l’analyse est acceptable (Sawyer et McCarthy,2005). Dans ce cas on peut répondre aux questions.
A-Facies hydrochimique.
- La formule ionique :
On classe les anions et cations par ordre croissant. Les anions en première ligne et les cations en deuxième ligne.
rHCO-3 rSO2- rCl-
rCa2+ rMg2+ r(Na+ +K+)
Selon cette formule le facies est bicarbonate calcique (HCO3-Ca).
B- On peut déterminer le facies hydrochimique a l’aide des graphiques (voir cours).
- Diagramme Schoeller- Berkaloff
Il s’agit de projeter les données en méq/L ou mg/L sur des bâtonnets. Pour la lecture il faut prendre les valeurs les plus élevées entre cations et anions.
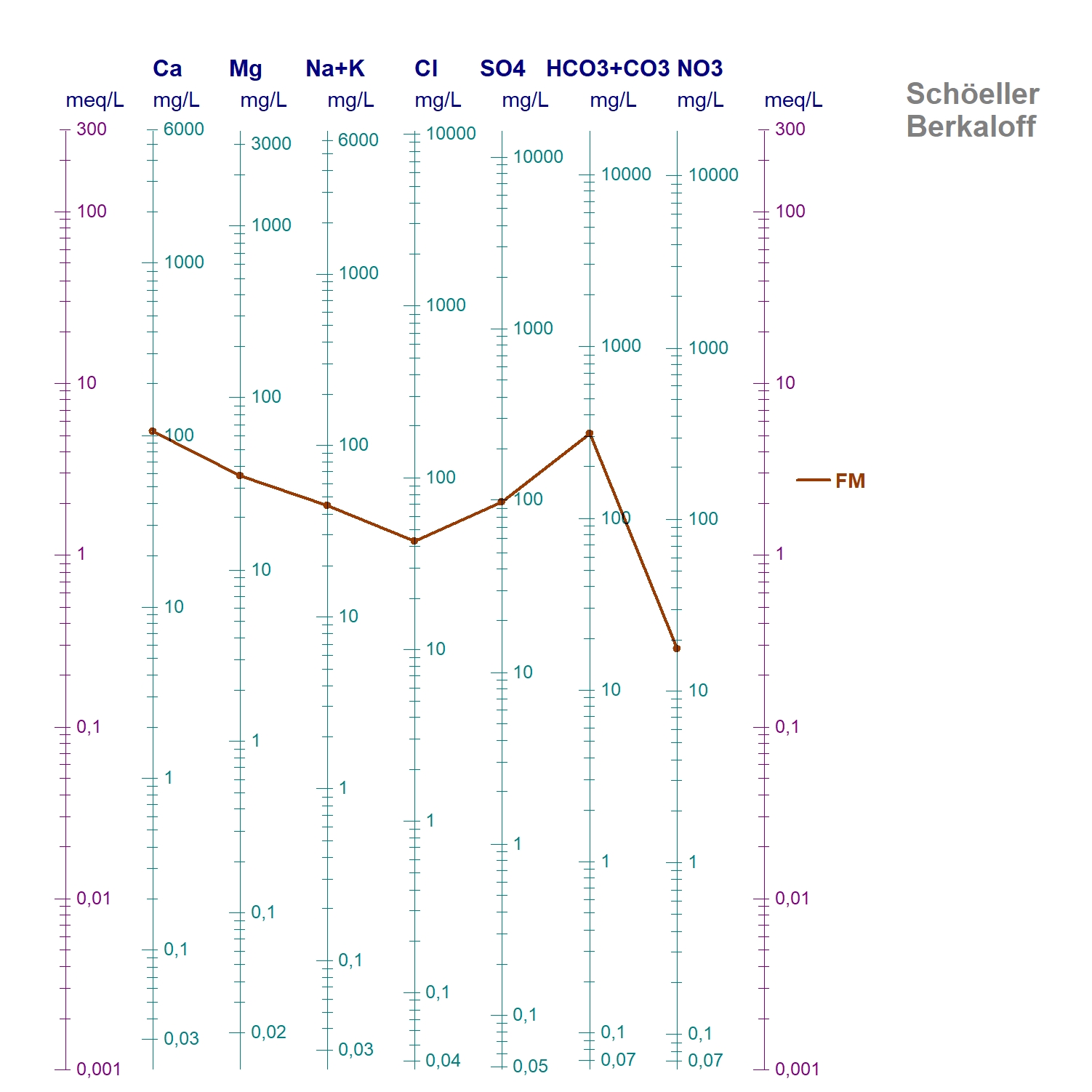
La lecture du facies se fait sur le losange. Il en ressort du diagramme que le facies est bicarbonate calcique (HCO3-Ca). Ce facies est du probablement a la dissolution des calcaires ou altération des silicates.
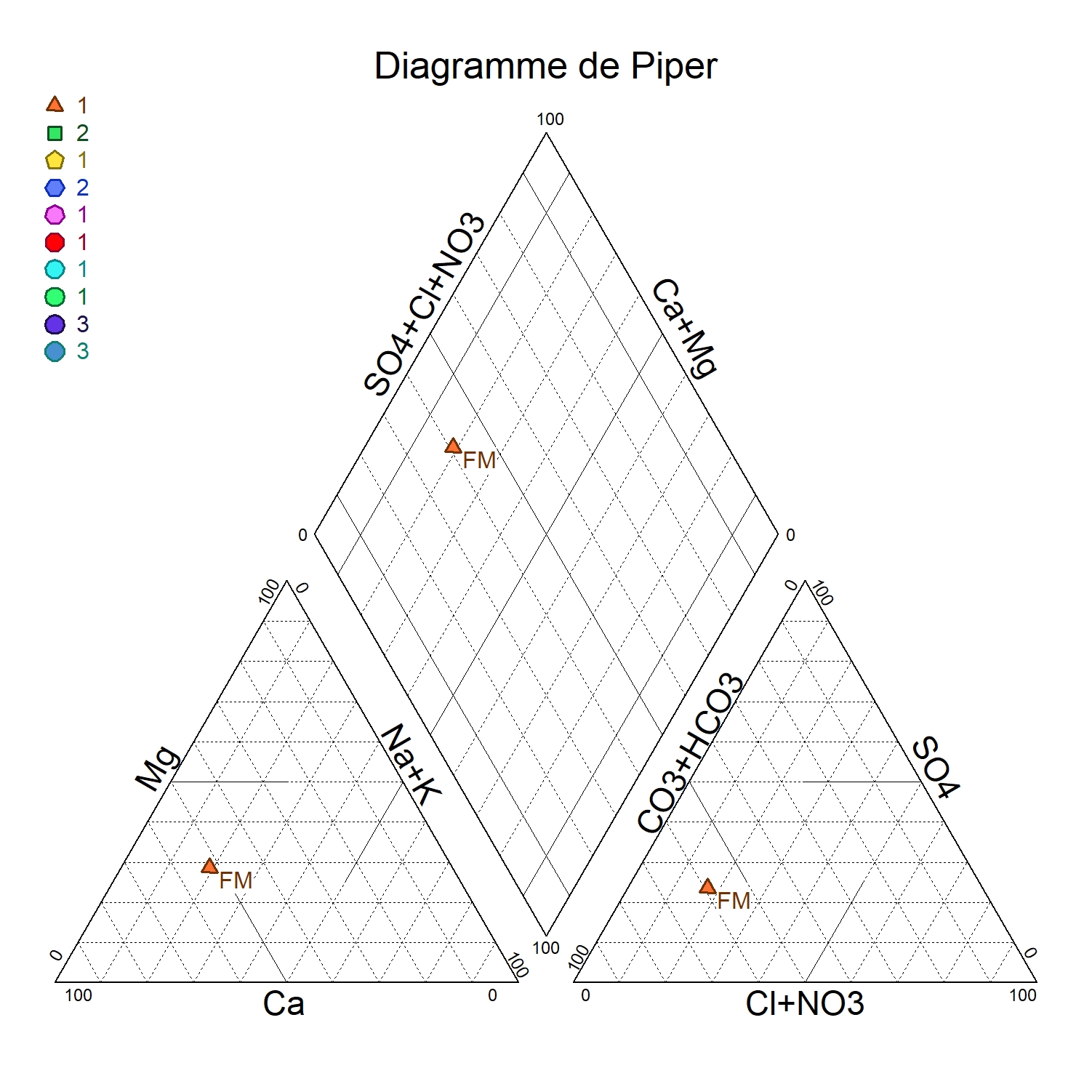
B-)
Détermination du Titre Hydrotimétrique (TH)
On le détermine à l’aide de Swayer-McCarty (1967)
TH (CaCO3) mg/ l= (Ca2++ Mg2+) méq/l x50
Ca2+ = 5.30 méq/l et Mg2+ = 2.91 méq/l d’où TH =410.50 mg/l
s. Les valeurs
Table 1 Classification des eaux basée le TH(CaCO3 (mg/l)) calculée est e 410.50 mg/l
Classification des eaux basée sur le TH (Swayer –McCarty)
<75 eau douce
75–150 Moyennement dure
150–300 dure
> 300 très dure
Selon cette classification, l’eau du forage est dure à très dure. Une eau dure n’est en rien nocive mais provoque quelques désagréments : mousse moins au savon, implique la formation de tartre avec obturation des canalisations.
C-) Comparason des donées analytiques avec les normes de l’OMS 2017)
Selon la norme de l’OMS ; l’eau est bonne qualité a l’exception des bicarbonates. La correction de l’eau s’impose.
La classification de TDS selon Freeze and Cherry (1979),
<1000 eau Fraiche
1000–10000 eau saumâtre
10000–100000 eau salée
>100000 eau très salée
Selon cette classification ; l’eau est fraiche ou douce. Selon ce paramètre l’eau est bonne à la consommation humaine.
Qualité de l'eau pour l’irrigation
La conductivité électrique est une bonne mesure du risque de salinité pour les cultures car elle reflète le TDS dans les eaux souterraines. le taux de salinité réduit l'activité osmotique des plantes et interfère ainsi avec l'absorption de l'eau et des nutriments du sol. Selon La conductivité électrique (864 uS/cm); cette eau est bonne pour l’irrigation (voir tableau).
Classification de la Qualité de l'eau d'irrigation basée sur la conductivité électrique (CE)
EC (uS/cm)
< 250 Excellent
250–750 bonne
750–2000 médiocre
2000–3000 Mauvaise
>3000 Inutilisable
SAR Sodium adsorption ratio (SAR)
Le taux d'adsorption du sodium (SAR) est un paramètre important pour déterminer l’utilisation pertinence de l'eau souterraine pour l'irrigation, car il s'agit d'une mesure du risque alcalin / sodium pour les cultures. SAR est défini par :
SAR = (Na+ +K+) / [(Ca2+ + Mg2+)1/2] / 2=1.94/ [(5.30+2.91)1/2/2=1.43
L’échantillons appartient à la classe des faibles teneurs en sodium (S1 ayant la valeur SAR de 10,67 l'eau ). Cela implique qu'aucun risque d'alcali n'est prévu pour les cultures. Si la valeur SAR est supérieure à 6 à 9, l'eau d'irrigation sera causée des problèmes de perméabilité sur les types de sols argileux qui rétrécissent et gonflent.
La donnée analytique tracées sur le diagramme de Richards ; montre que l’échantillon d'eau est dans la classe de C2S1, indiquant une faible salinité et une faible teneur en eau en sodium, qui peut être utilisées pour l'irrigation. voir diagramme a la fin du texte
Taux de sodium (Na %)
Le Taux de sodium (Na %) est calculé l’aide de la formule donné ci-dessous :
(Na++K+) % =(Na++K+) x100/ (Ca 2+ +Mg2+ +Na++K+)
(Na++K+) %=1.94 x100/10.15= 19.11%.
Selon ce critère, l’eau appartient à la classe 1. L’eau est excellente pour être utilisée à l’irrigation
Classification des eaux souterraines à l'irrigation sur la base du pourcentage de sodium % Na
% Na classe
<20 Excellente
20–40 bonne
40–60 médiocre
60–80 mauvaise
>80 inutilisable
Remarque
Lorsque la concentration de sodium est élevée dans l'eau d'irrigation, les ions sodium ont tendance à être absorbés par les particules d'argile, déplaçant les ions Mg2 + et Ca2 +. Ce processus d'échange de Na+ dans l'eau contre Ca2+ et Mg2+ dans le sol réduit la perméabilité et conduit finalement à un sol avec un mauvais drainage interne. Par conséquent, la circulation de l'air et de l'eau est limitée par temps humide et ces sols sont généralement durs lorsqu'ils sont secs.
Carbonate de sodium Résiduel (RSC)
La somme excessive de carbonate et de bicarbonate dans les eaux souterraines par rapport à la somme de calcium et de magnésium influence également l'inadéquation d'eaux souterraines pour l'irrigation. Il s'agit du carbonate de sodium résiduel (RSC), qui est calculé comme suit (Ragunath 1987) :
RSC = (HCO3+CO3) - (Ca2+ +Mg 2+)
Si on n’a pas de valeur de CO2-3 ; on multiplie La valeur de HCO3 exprimée en mg/l par 0.3 d’où la nouvelle formule :
RSC = (HCO3x0.33) - (Ca2+ +Mg 2+)
Ca2+ et Mg2+ sont exprimés en méq/l. Dans
notre cas ; on utilise la seconde formule.
RSC = (312x 0.333) - (5.30+ +2.91) =-4.32 (meq/l
La classification des eaux d'irrigation selon la classification du RSC est mentionnée ci- dessouse
RSC (meq/l)
classe
<1.25 bonne
1.25–2.5 mauvaise
>2.50 inutilisable
Le RSC calculé appartient à la classe 1. L’eau est utilisée à l’irrigation sans restriction.
Indice de perméabilité
Les valeurs de l'indice de perméabilité (PI) indiquent également que les eaux souterraines conviennent à l'irrigation. Il est défini comme suit (Ragunath 1987):
IP = (Na+ +( HCO-3)1/2 x100 /(Ca +Mg +Na+K)=4.20/10.15=0.22x100=22%
où les concentrations sont rapportées en meq / l. L'IP est
22% à 86,3%, qui fait partie de la classe 1 du graphique de Doreen (voir
cours). Dans notre cas l’eau est bonne pour l’irrigation.
Mg2+ Ratio
Ce paramètre a été développé par Paliwal (1972) et est defini comme suit ;
Mg2+ Ratio = 100 (Mg2+ / (Ca2+ +Mg2+)1/2
Les concentrations de Ca2+ et Mg2+ sont exprimées en méq/l
Mg2+ Ratio = 100 (2.91/ (5.30+2.91/2)1/2=100(2.91/2.022=144 %
La valeur De Mg ratio calculée est 144%. Cette valeur est supérieure à 50%, ce qui indique un effet défavorable sur le rendement des cultures et augmentation de l’alcalinité du sol. Si Mg2+ ratio est inférieure a 50% ce qui correspond à la limite tolérée, ce qui traduit un effet favorable sur le rendement des cultures et diminution de l’alcalinité.
Diagramme de Richards
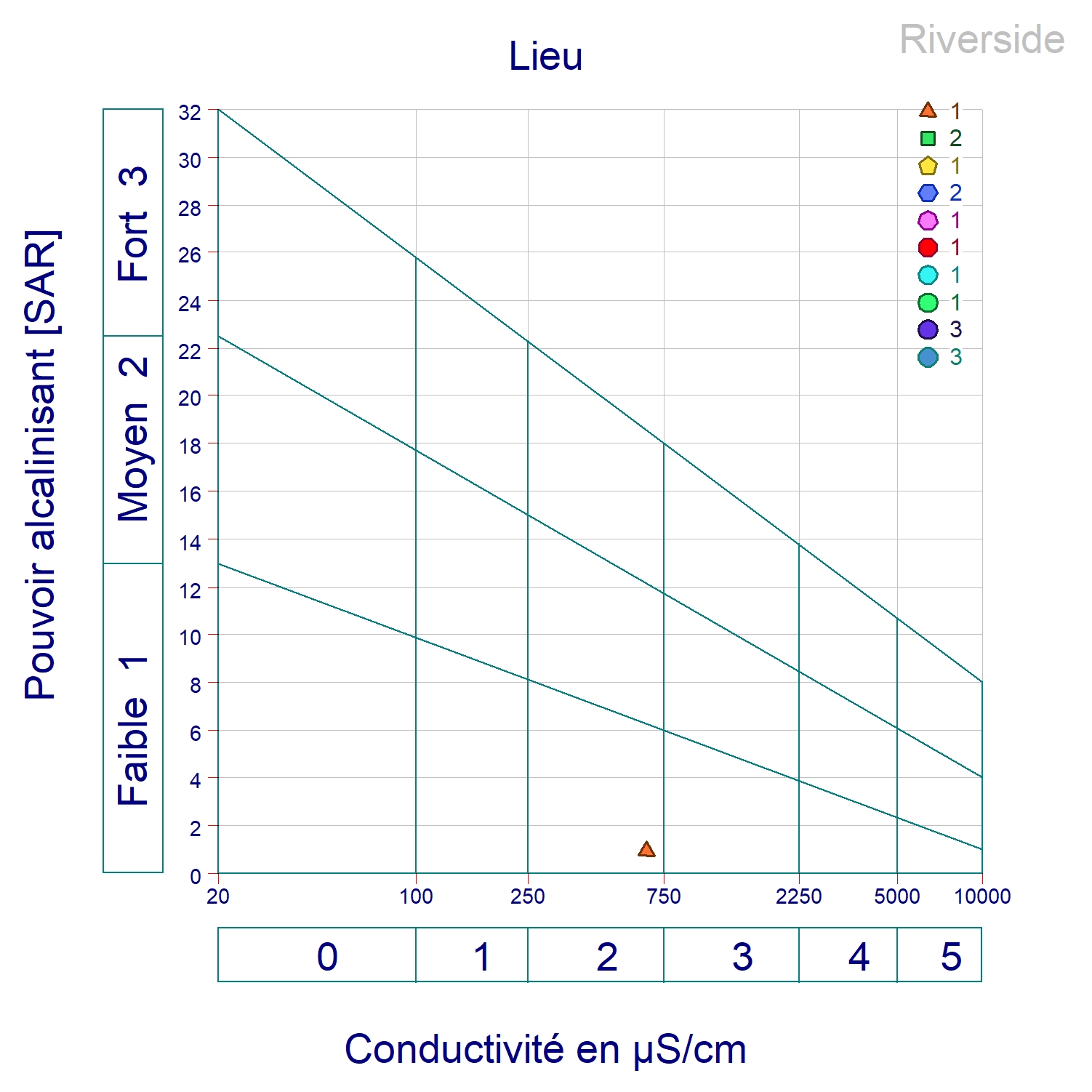
Dans notre cas ; Les données sont projeté sur ce diagramme points appartiennent a la classe C1 S1 ce signifie que l’eau peu être utilisée à l’irrigation sans restriction figure ci -dessous.
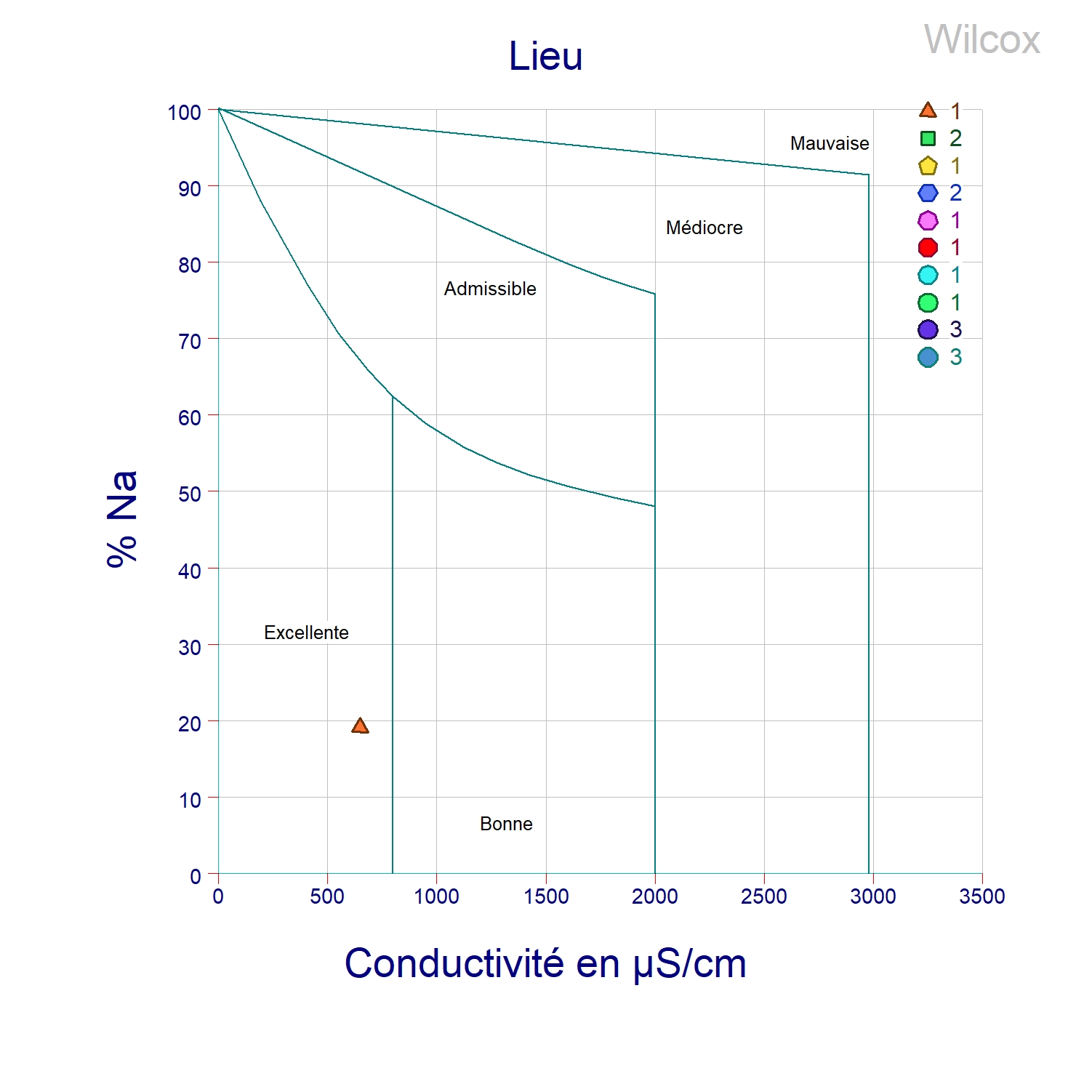
Diagramme de wilcox
Si l’eau est très riche en sodium, il ‘ y a risque de sodicité (intoxication des plantes) et aussi il y a risque sur la perméabilité du sol. La projection de la CE en fonction du taux de sodium montre que l’eau du forage appartient à la classe excellente. Il n’y a pas de risque de sodicité ni sur la perméabilité du sol. Figure ci-dessous
Utilisation industrielle
Pour l’Utilisation industrielle, on peut determiner le ∆pH et est donnée par la formule suivante.
∆pH= pH-pHS
pH = pH de l’echantillon
pHS = pH de saturation ou d’equilibre
Application
∆pH= 7.40-7.65 = -0.25
Si ∆pH<0 eau agressive
Si ∆pH>0 eau incrustante ou entartrente
Dans notre cas , l’eau est agressive vis vis des carbonates cad les carbonates pricipités sont aussitôt repris par la dissolution.
Indice de Ryznar
Il est donné par la relation suivante
IR = 2 pHS –pH
Si IR=6 eau neutre
Si IR>6 eau entartrente ( dépôt de tartre ou dépôt de calcaire dans les conduites et chaudières)
Si IR<6 eau agressive
Application numerique
IR = 2x7.65 -7.40 =15.30- 7.40 =7.90
IR >6 eau agressive
Fin
- المعلم: TAHAR NOUAR